В тази статия са обединени четирите публикации на Пол Жамине и неговата съпруга относно рисковете при нулев прием на въглехидрати, като трябва да се има предвид, че под "нулев прием" те разбират прием на въглехидрати само от зеленчуци, без да се включват плодове или скорбялни храни. За всяко от твърденията са представени доказателства. Разбира се, винаги може да се намерят и други гледни точки. Но тъй като това са често срещани проблеми, е полезно да се прочете и гледната точка на Жамине.
Рискове при нулев прием на въглехидрати, част І: Възможно ли е да съществува въглехидратен дефицит?
Рискове при нулев прием на въглехидрати, част І: Възможно ли е да съществува въглехидратен дефицит?
Автор: Пол Жамине
В блоговете на палео тематика често се казва, че
въглехидратите не са необходими. Ето един пример от блога на Don Matesz - автор на отлични статии, чийто начин
на хранене е изключително близък до нашия:
Белтъчините са
есенциални, но въглехидратите не са… Не можете да ограничавате белтъчините
прекалено много, но можете да ограничите въглехидратите драстично.
Д-р Майкъл Идс се изказва с насмешка по отношение на идеята за болестно състояние, дължащо
се на дефицит на въглехидрати:
Съществуват ли
заболявания поради дефицит на въглехидрати, г-н Харпър, които да са известни на
Вас, но не и на останалите специалисти по хранене?
Ще Ви подскажа: не съществуват.
Но има
заболявания, причинени от дефицит както на мазнини, така и на белтъчини, за
които пише във всеки учебник по вътрешни болести.
Тези изявления ме впечатлиха, когато започнах да спазвам
палео хранене преди пет години. Но след няколко години и няколко
здравословни проблема осъзнах, че това схващане е погрешно.
Защо не са
известни болестните състояния, които се дължат на дефицит на въглехидрати?
Как лекарите откриват, че съществува определено
заболяване, породено от дефицит на хранителни вещества?
Не е толкова лесно, колкото може би си мислите. Например
съществуването на заболявания вследствие на дефицит на незаменими мастни
киселини при хората е било под съмнение чак до 50-те години, въпреки че
дефицитът на омега-6 е бил установен и описан при плъхове през 20-те. [1] Причината е,
че дефицитите на омега-6 и омега-3 могат да възникнат само при неестествен
начин на хранене. Съществуването на дефицита на омега-6 при хора е доказано в крайна сметка
при бебета, хранени с обезмаслено адаптирано мляко през 40-те и 50-те.
Две обстоятелства са затруднили установяването в науката
на синдрома на въглехидратния дефицит:
- Липса на животински модел.
- Рядко срещаният нулев прием на въглехидрати при хора.
Доскоро малко хора, освен инуитите, са се хранели
стриктно нисковъглехидратно, а инуитите не са оставили надеждни медицински архиви. Вследствие на това
хората, за които е доказано, че са развили синдроми на въглехидратен дефицит,
са малко или напълно липсват.
Това не би било проблем, ако беше възможно да се
провокира въглехидратен дефицит при животни.
Но не е възможно.
Животните не развиват въглехидратен дефицит, защото
мозъкът им е малък, което означава ниски нужди от глюкоза, а черният им дроб е
голям, което пък предполага висока способност за синтез на глюкоза. Те могат да
произведат цялата глюкоза, която им е необходима, от белтъчини или от летливи
киселини като пропионат, получени чрез бактериална ферментация в храносмилателния
им тракт.
Но както отбелязваме в книгата си, хората са по-уязвими.
Ние имаме малък
черен дроб и голям мозък, поради което възможността за възникване на глюкозен
дефицит е реална.
Ето сравнение между размерите на мозъка, черния дроб и
храносмилателния тракт при хората и други примати [2]:
Орган
|
% от телесното
тегло, хора
|
% от телесното
тегло, други примати
|
Мозък
|
2,0
|
0,7
|
Черен дроб
|
2,2
|
2,5
|
Храносмилателен
тракт
|
1,7
|
2,9
|
Мозъкът е най-значимият фактор, който определя нуждите от
глюкоза. При другите примати нуждата от енергия, идваща от глюкоза
или кетони, е около 7% от общите енергийни нужди, но при хората е около 20%.
В сравнение с другите примати хората имат 12% по-малък
черен дроб. Това означава, че не можем да произведем същото количество глюкоза от
белтъчини като другите животни. Хората имат 40% по-малък
храносмилателен тракт. Това означава, че не можем да произведем много късоверижни мастни киселини (които
осигуряват кетони или субстрат за глюконеогенеза) от фибрите.
Затова, макар че животните могат да посрещнат малките си
нужди от глюкоза (5% от дневните калории) чрез големия си черен дроб, хората
може да не са в състояние да посрещнат големите си нужди от глюкоза (20-30% от необходимите
дневни калории) с малкия ни черен дроб.
Следователно, ако съществуват болестни състояния
вследствие на въглехидратен дефицит, те ще засегнат само хората, а не
животните.
За какво да
следим, за да установим дали страдаме от въглехидратен дефицит?
За да се установи наличието на синдром на въглехидратен
дефицит при хората, трябва да разгледаме популации с много нисък прием на
въглехидрати като:
- инуитите при традиционния им начин на хранене, базиран на лова;
- пациентите, страдащи от епилепсия, които се лекуват с кетогенна диета;
- спазващите Оптималната диета в Полша, които се придържат към стриктен нисковъглехидратен хранителен режим от над 20 години;
- спазващите стриктно нисковъглехидратно хранене в други държави, които са започнали да се хранят по този начин през последните 10 години, откакто палео движението започна да набира скорост.
Също така трябва да имаме представа какви симптоми да
търсим. Консумиращите най-много глюкоза части на тялото са:
- мозъкът и нервите;
- имунната система;
- храносмилателният тракт.
Организмът полага големи усилия да гарантира достатъчна
енергия за мозъка и нервната система, затова съществува най-голяма вероятност
дефицитът на глюкоза да засегне имунната и храносмилателната функция.
И така, очертали сме нашия проект.
През следващата
седмица или колкото дълъг период е необходим, докато ни омръзне, ще проучваме
доказателствата за наличие на болестни състояния при хората, породени от въглехидратен
дефицит.
Статии по темата
Други статии от тази серия:
- Dangers of Zero-Carb Diets, II: Mucus Deficiency and Gastrointestinal Cancers A.
- Danger of Zero-Carb Diets III: Scurvy .
- Dangers of Zero-Carb Diets, IV: Kidney Stones.
Източници
[1] Holman RT. The slow discovery of the importance of
omega 3 essential fatty acids in human health.
J Nutr. 1998 Feb;128(2 Suppl):427S-433S. http://pmid.us/9478042
[2] Aiello LC, Wheeler P. The expensive tissue
hypothesis: the brain and the digestive system in human and primate evolution. Current Anthropology 1995(Apr); 36(2):199-211.
Рискове при нулев
прием на въглехидрати, част ІІ:
Недостиг на слуз и възникване на злокачествени образувания на
храносмилателната система
Автор: Пол Жамине
Ян Квашниевски е разработил своята Оптимална диета преди
около 40 години и тя е придобила изключителна популярност в Полша.
Квашниевски препоръчва зрелите хора да приемат следните
пропорции макронутриенти:
60 г белтъчини – 180 г мазнини – 30 г въглехидрати
(Източник).
(Източник).
От гледна точка на калории това се равнява приблизително
на 240 калории от белтъчини / 1640 калории от мазнини / 120 калории от
въглехидрати при дневен прием на 2000 калории.
Съотношенията в създадената от нас Диета за перфектно
здраве (The Perfect Health Diet) са по-скоро 300 калории от белтъчини / 1300
калории от мазнини / 400 калории от въглехидрати. Следователно двата хранителни режима
биха били сходни, ако вземем около 300 калории, т.е. 15% от енергията, от
мазнините и ги добавим към въглехидратите под формата на глюкоза/скорбяла (а не
фруктоза/захар!).
Обърнете внимание, че ние препоръчваме да набавяте
минимум 600 калории на ден от белтъчини и въглехидрати заедно. Така се гарантира
достатъчно протеин за синтез на глюкоза и кетони в черния дроб. Но Оптималната
диета препоръчва само 360 калории общо (и по-малко при жените), което показва,
че глюконеогенезата не може напълно да компенсира дефицита на глюкоза, идваща
от храната, дългосрочно.
В нашата книга ние отбелязваме, че здравият организъм в
типичния случай оползотворява и се нуждае от около 600 калории от глюкоза на
ден. В клиничното изпитване Bellevue All-Meat Trial, проведено през 1928 г.,
Вилялмур Стефансон е приемал 550 калории от белтъчини на ден, което вероятно е
добра приблизителна оценка за минималното количество, което е необходимо да се
приема, за да се предотврати загуба на мускулна маса при нулев прием на
въглехидрати.
Ако се приемат само 360 калории от въглехидрати +
белтъчини на ден, Оптималната диета предполага задължително влизане в кетоза,
ако мускулната маса трябва да бъде запазена.
Тъй като максимум
200 до 300 калории на ден от необходимите калории от глюкоза могат да бъдат
заместени от кетони, Оптималната диета предполага съществуване на ръба на
глюкозния дефицит.
Злокачествени
образувания на храносмилателния тракт при спазващите Оптималната диета
От блога на Питър научих, че тревожно голям брой от
спазващите Оптималната диета умират от различни видове рак на храносмилателната
система. Наскоро Адам Яни, президент на OSBO (полската асоциация за спазващите
Оптималната диета), е починал от рак на стомаха на 64-годишна възраст, след
като е спазвал диетата в продължение на 17 години.
Преди това Карол
Браниек, друг от водачите на OSBO, е починал на 68-годишна възраст от рак на
дванадесетопръстника.
Един поляк, който в миналото е спазвал Оптималната диета,
а сега е преминал на Диетата за перфектно здраве, отбелязва, че злокачествените
образувания на храносмилателния тракт изглежда са често срещани сред спазващите
Оптималната диета:
Оставаме с
впечатлението, че случаите на рак на храносмилателната система, включително на
стомаха, дванадесетопръстника, дебелото черво, са доста често срещани… [източник]
Искам да обясня каква е причината според мен, защото
опасността, която спазващите Оптималната диета откриват, беше един от основните
фактори, които ни накараха да формулираме и публикуваме Диетата за перфектно
здраве.
Нулевият прием на
въглехидрати може да причини недостиг на слуз
Спазвах диета с високо съдържание на зеленчуци, но крайно
нисковъглехидратна от декември 2005 г. до януари 2008 г. Тогава мислех, че
приемам 300 калории от въглехидрати на ден, но сега смятам, че приемът ми на
въглехидрати е бил нулев, защото не мисля, че повечето зеленчуци могат да бъдат
източник на въглехидрати. Въглехидратите, идващи от зеленчуци, се
консумират предимно от чревните бактерии, от чиято помощ се нуждаем, за да
разградим зеленчуците, или от чревните клетки, които използват глюкоза по време
на процеса на храносмилане.
През цялото време, докато спазвах този нулев прием на
въглехидрати, имах сухота на очите и устата.
Очите ми бяха
кръвясали и раздразнени, и се наложи да се откажа от контактните лещи. С помощта на
неколкократни експерименти установих, че за сухотата на очите ми допринасят два
фактора – дефицит на витамин С и глюкозен дефицит.
След като реших
проблема с витамин С, експериментирах към 50 пъти през следващите няколко
години, като повишавах приема си на въглехидрати, което довеждаше до изчезване
на сухотата в очите, а после отново ограничавах въглехидратите и сухотата
веднага се връщаше. Това доказа категорично, че причината за сухотата на очите беше глюкозен
дефицит.
Ребека споделя за сходни симптоми при себе си и своите приятели, хранещи се
нисковъглехидратно.
Това е добре известен симптом и при гладуващи. Както се отбелязва
в преглед на публикации, цитиран от ЛинМари Дейвис (и към който е даден линк от CarbSane в коментарите),
Тъй като запасите
от гликоген в черния дроб се изчерпват в рамките на 24 часа при гладуване, след
това концентрациите на кръвната глюкоза се поддържат изцяло чрез
глюконеогенеза. Тя разчита на първо място на разграждане на протеин (малко количество идва
от глицерола, който се освобождава при липолизата – разграждането на мазнини) и
следователно води до загуба на мускулна маса.
Именно ефектите на
белтъчното недохранване водят в крайна сметка до неспособност за откашляне и
поддържане на чисти дихателни пътища, което пък води до пневмония и
смърт при продължително гладуване; хипогликемия не се наблюдава.
[1]
Друг често наблюдаван симптом при крайно
нисковъглехидратните диети е запекът. Той често се обяснява с недостатъчен
прием на фибри, но аз съм скептичен към това обяснение.
Ще засегна
различните възможни причини за запек в бъдеща статия, но засега само ще посоча,
че недостатъчното количество слуз в храносмилателния тракт би довело до сухота
на дебелото черво и би причинило запек.
Каква е връзката между нулевия прием на въглехидрати и
сухотата на очите, устата, дихателните пътища и храносмилателния тракт?
Сълзите, слюнката и слузта в синусите, дихателните пътища
и храносмилателния тракт се състоят основно от гликопротеини, наречени муцини. Муцините са
съставени на първо място от захар; в обичайния случай те са изградени от редица
дълги вериги от захари, свързани с белтъчен гръбнак.
Например, основният муцин в храносмилателния тракт, MUC2,
е съставен от димеризирани белтъци – всеки белтък поотделно тежи 600 000
далтона, т.е. всяка двойка тежи 1,2 млн. далтона – плюс към 4 млн. далтона
захар, което означава обща маса 5 млн. далтона.
В слузта тези
големи молекули се свързват кръстосано, за да образуват „огромни мрежоподобни
ковалентни полимери“. [източник]
Ако поради каквато и да било причина производството на
слуз бъде прекратено заради недостиг на глюкоза, не бихме имали сълзи, слюнка и
слуз в храносмилателния тракт и дихателните пътища.
Недостатъчната
слуз причинява рак
Между недостига на слуз и злокачествените тумори на
храносмилателния тракт има силна връзка.
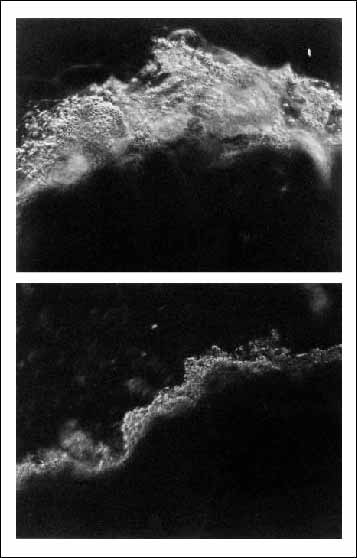
H. pylori е най-значимият известен рисков фактор за възникване на рак на стомаха. [2] Инфекцията с H.
pylori се открива при около 80% от случаите на този рак. [3] Едната
причина, поради която H. pylori благоприятства възникването на рак на
стомаха в толкава висока степен, може би е, че намалява количеството слуз в
стомаха, както тази снимка показва:
Горе: Нормална стомашна лигавица Долу: Стомашна лигавица
при човек, заразен с H. pylori
Учените са създали порода мишки, при които липсват гени
за основните муцини в храносмилателния тракт.
Те осигуряват
преки доказателства за това как недостигът на слуз влияе върху развитието на
рак.
Експерименти при мишки с нокаут/нокдаун на гена Muc1 са
показали, че при инфекция с Helicobacter, мишките, при които липсва
Muc1, развиват много по-мащабно възпаление, благоприятстващо възникването на
рак, отколкото нормалните мишки. [4]
Основният муцин в червата е Muc2. Екипът на Леонард
Аугенлихт от Центъра за изучаване на рака „Алберт Айнщайн“ в Ню Йорк е изучавал
мишки, при които липсва генът Muc2. Те развиват рак на дебелото черво.
[5]
Ако проследим процеса една стъпка назад до причината за
дефицита на муцин, захарите в муцина са изградени от по-малки частици, наречени
О-гликани. Доказано е, че мишките, при които О-гликаните липсват, са склонни да
развият рак на дебелото черво. „Мишките с дефицит на C3GnT проявиха дискретно,
специфично за дебелото черво понижение в нивата на белтъка Muc2, и повишена
пропускливост на чревната бариера. Освен това тези мишки бяха силно податливи
на експериментални причинители на колит и колоректален аденокарцином.“
[6]
Дефицитът на някои
хранителни вещества също може да играе роля
Някои хранителни вещества са необходими за производството
на муцин – а по-точно витамин D. [7, 8] Полша се намира сравнително на север и
много от спазващите Оптималната диета може да са имали ниски нива на витамин D.
Други важни микронутриенти за превенция на рака са йод и
селен. Установено е, че Полша в частност е имала най-ниския прием на йод и
най-високите нива на смъртност от рак на стомаха в Европа.
Откакто през 1996
г. Полша е започнала програма за задължителна йодна профилактика, броят на
случаите на рак на стомаха се е понижил:
В Краков
стандартизираният коефициент на заболеваемост от рак на стомаха при мъжете се е
понижил от 19,1 на 100 000 на 15,7 на 100 000, а при жените – от 8,3
на 100 000 на 5,9 на 100 000 в периода 1992 – 2004 г. Значително
намаляване на средната скорост на понижение е наблюдавано при мъжете и жените
(2,3%, съответно 4,0% годишно). [9]
Следователно повишеният риск за развитие на тумори на
храносмилателния тракт при спазващите Оптималната диета в Полша, причинен от
дефицит на муцин, може да е бил усложнен от дефицит на йод и недостатъчно
излагане на слънчева светлина.
Заключение
Здравословната диета не трябва да допуска дефицити. Оптималната диета
не е била замислена така, че да предотврати глюкозен дефицит.
Има сериозни основания да подозираме, че поне част от
спазващите Оптималната диета са развили дефицит на муцин вследствие на усилията
на организма да съхрани глюкозата и протеина.
Това би довело до
значително повишен риск за развитие на тумори на храносмилателния тракт. Следователно не е
изненадващо, че много спазващи Оптималната диета се разболяват от рак на храносмилателния
тракт след 15-20 години.
Ние препоръчваме прием на въглехидрати + белтъчини,
отговарящ на минимум 600 калории на ден, за да се избегне евентуален глюкозен
дефицит. Може да се предположи, че нулевият прием на въглехидрати при минимум 600
калории на ден от белтъчини за глюконеогенеза не би повишил риска за рак на
стомашночревния тракт толкова, колкото Оптималната диета.
Но защо да бъдете
опитното свинче, което ще изпробва тази идея? Организмът ви се нуждае от известно
количество глюкоза и със сигурност за него е по-малко стресиращо да му
осигурите това количество, отколкото да го принуждавате да синтезира глюкоза от
белтъчини.
Периодичното гладуване и нисковъглехидратните, кетогенни
диети имат терапевтичен ефект при различни заболявания.
Но всеки, който
спазва периодично гладуване или кетогенна диета, трябва внимателно да наблюдава
очите и устата си за признаци на понижено производство на слюнка или сълзи. Ако е налице
признак на сухота на очите или устата, режимът трябва да бъде прекъснат и да се
приеме известно количество глюкоза/скорбяла.
Оризът е добър
източник. Тревожно е не само, че можете да развиете рак след 15 години. Нормалната
лигавична бариера е от съществено значение и за защитата на храносмилателната
система и дихателните пътища от патогени.
Статии по темата
Други статии от тази серия:
- Dangers of Zero-Carb Diets, I: Can There Be a Carbohydrate Deficiency?.
- Danger of Zero-Carb Diets III: Scurvy .
- Dangers of Zero-Carb Diets, IV: Kidney Stones.
Източници
[1]
Sonksen P, Sonksen J. Insulin: understanding its action in health and disease.
Br J Anaesth. 2000 Jul;85(1):69-79. http://pmid.us/10927996.
[2]
Peek RM Jr, Crabtree JE. Helicobacter infection and gastric neoplasia. J
Pathol. 2006 Jan;208(2):233-48. http://pmid.us/16362989.
[3]
Bornschein J et al. H. pylori Infection Is a Key Risk Factor for Proximal
Gastric Cancer. Dig Dis
Sci. 2010 Jul 29. [Epub ahead of print] http://pmid.us/20668939.
[4]
Guang W et al. Muc1 cell surface mucin attenuates epithelial inflammation in
response to a common mucosal pathogen. J Biol Chem. 2010 Jul
2;285(27):20547-57. http://pmid.us/20430889.
[5]
Velcich A et al. Colorectal cancer in mice genetically deficient in the mucin
Muc2. Science. 2002 Mar 1;295(5560):1726-9. http://pmid.us/11872843.
[6]
An G et al. Increased susceptibility to colitis and colorectal tumors in mice
lacking core 3-derived O-glycans. J Exp Med. 2007 Jun 11;204(6):1417-29.
http://pmid.us/17517967.
[7]
Paz HB et al. The role of calcium in mucin packaging within goblet cells. Exp
Eye Res. 2003 Jul;77(1):69-75. http://pmid.us/12823989.
[8]
Schmidt DR, Mangelsdorf DJ. Nuclear receptors of the enteric tract: guarding
the frontier. Nutr Rev. 2008 Oct;66(10 Suppl 2):S88-97. http://pmid.us/18844851.
[9]
Go?kowski F et al. Iodine prophylaxis–the protective factor against stomach
cancer in iodine deficient areas. Eur J Nutr. 2007 Aug;46(5):251-6. http://pmid.us/17497074.
Рискове при нулев
прием на въглехидрати, част ІІI:
Скорбут
Автор: Пол Жамине
Започнах да спазвам нисковъглехидратен палео режим в края
на 2005 година. Ядях много зеленчуци, но бях изключил напълно скорбялните храни
и почти не консумирах плодове. Като погледна назад, бих казал, че
въглехидратният ми прием е бил почти нулев.
По това време вече
от 12 години страдах от хронично заболяване, което се влошаваше леко с всяка
изминала година и беше пълна загадка за мен.
Когато започнах да
се храня нисковъглехидратно, веднага забелязах промени:
симптомите, които
много по-късно щях да разпозная като дължащи се на хронична бактериална
инфекция, се облекчиха (в част от тялото ми, но не в мозъка), а една хронична
гъбична инфекция се влоши.
След около година развих скорбут.
За мой срам ми
отне много дълго време да се досетя за какво става въпрос.
Докато осъзная
какъв е проблемът, вече имах 3 кариеса; бях свалил 12 килограма; бях развил
дивертикулит, а коремната ми аорта видимо се издуваше при всеки удар на сърцето
ми; освен това имах ранички по кожата - драскотини и ожулвания - които от 6
месеца не зарастваха.
Това, че развих скорбут, беше изненада за мен, защото
консумирах много зеленчуци и приемах мултивитамин, съдържащ 90 мг витамин С.
Никога не бях имал признаци на дефицит на витамин С, преди да мина на
нисковъглехидратно хранене.
С прием на четири грама витамин С на ден в продължение на
два месеца се отървах от всички симптоми на скорбут.
Щяха да минат още
няколко години, докато се досетя за причините за инфекциите, но това
преживяване ме научи колко важни са микронутриентите.
То ме убеди в
нуждата да се запозная подробно с различните хранителни режими и науката за
храненето, и така двамата със съпругата ми започнахме да пишем книгата си Диета за перфектно здраве (Perfect
Health Diet).
Скорбут при
кетогенно хранене
Аз не съм единственият, който е имал такова преживяване. Ето един случай,
който споменаваме в книгата: историята на момиче с епилепсия.
К. М. била 9-годишно
момиче… на което на 6-месечна възраст била поставена диагноза епилепсия. Започнала
кетогенна диета през октомври 2003 г., защото множеството противоепилептични
лекарства, които приемала, не й действали - имала по цели 12 тонични гърча на
ден и продължителни периоди на неконвулсивен статус епилептикус. След като й била
предписана тази диета, честотата на пристъпите се понижила чувствително и имало
редица дълги периоди, в които изобщо не получавала пристъпи.
Майката на К. М.
разказа, че дъщеря й страдала от кървене на венците от началото на септември
2006 г.. Описа ги като тъмночервени, подути и кървящи.
Освен това обясни,
че К. М. имала корички от засъхнала кръв около устата.
Зъболекарят на
семейството предположил, че причината са никнещи зъби и препоръчал К. М. да
използва гел с 0,2% хлорхексидин глюконат и да продължи да спазва обичайния си
режим на устна хигиена, но мерките не дали резултат.
Около месец
по-късно дясната ръка на пациентката се подула.
Помислили, че е
счупена или изкълчена, но от ортопедичната клиника на болницата я изписали,
защото било налице клинично подобрение, а рентгеновите снимки не показвали
образуване на калуси.
В началото на ноември
в трахеята на К. М. попаднал млечен кътник, докато почиствали зъбите й (фиг. 1.) Била
необходима спешна бронхоскопия, за да го извадят. Хирурзите извадили й
останалите й млечни зъби, за да се избегне повторно възникване на същия
проблем...
Тогава й бил
записан час за консултация в детска стоматологична клиника към Стоматологичния
университет на Лийдс. Но тя така и не отишла, защото около три седмици след
изваждането на млечните зъби К. М. била приета в болницата със субфебрилна
температура, постоянно кървене на венците, оток на ръцете и ходилата и петехиален
обрив по краката. [1]
Момичето приемало обичайното количество витамин С чрез
храната: дневният й прием бил изчислен на 73 мг/ден, далеч над препоръчвания дневен
прием за деца на 9-13 годишна възраст в САЩ, който е 45 мг/ден. Въпреки това
серумното й ниво било едва 0,7 микромола/литър.
Диагнозата скорбут
се поставя при нива под 11 микромола/литър.
Симптомите на скорбут се появяват толкова неусетно, че е
лесно да бъдат пропуснати. В случая с К. М. един специализант от
Индия случайно разпознал симптомите. Иначе може би на лекарите никога е
нямало да им хрумне да изследват нивото й на витамин С.
[2]
Каква е причината
за скорбута при нисковъглехидратно хранене?
И така, каква е причината за развитие на скорбут при
нисковъглехидратно хранене, дори ако приемът на витамин С е далеч по-висок от
препоръчваният в САЩ?
Изглежда причината е едновременното действие на два
фактора:
- инфекция или някаква друга форма на стрес (напр. травма, рак) води до окисляване на извънклетъчния витамин С; и
- при хранене, водещо до ниски нива на инсулин или до дефицит на глутатион, окисленият витамин С не се рециклира.
Инфекциите и
витамин С
Имунният отговор на инфекции поражда реактивни кислородни
видове, които окисляват витамин С. Окислението води до това, че витамин С губи
един водороден атом и се превръща в „дехидроаскорбинова киселина“ или DHAA. Ако DHAA остане в
кръвта, тя се разгражда, като полуживотът й е 6 минути.
[3]
Инфекциите могат да доведат до дефицит на витамин С при
всякакъв начин на хранене. По време на т. нар. „отговор на острата
фаза“ срещу инфекция или травма често се стига до дефицит на витамин С. Ето една хубава
публикация от проучване, в което френски лекари изследвали пациентите си в
болницата за скорбут:
Измерихме
серумното ниво на аскорбинова киселина (SAAL) и проверихме за клинични и
биологични признаци на скорбут при 184 пациенти, хоспитализирани в рамките на
2-месечен период.
РЕЗУЛТАТИ: Честотата на
хиповитаминоза С (понижени запаси: SAAL<5 span=""> SAAL<2 47="" span=""> Около 16,9% от пациентите имаха дефицит на витамин С.
Налице беше силна
асоциация между хиповитаминоза С и наличие на отговор на острата фаза (p=0,002).
[4]
Следователно половината пациенти имали понижени запаси от
витамин С, а 17% имали откровен дефицит, който би довел до скорбут, ако не бъде
некоригиран.
И по-рано сме писали колко важно е да се приема витамин С
по време на инфекции:
- „Борба с вирусните инфекции чрез прием на витамин С в максималната поносима доза“ http://perfecthealthdiet.com/?p=636.
- „Новозеландец обявен за мъртъв от лекарите, излекуван с витамин С“, http://perfecthealthdiet.com/?p=439 и „Витамин C срещу съвременната медицина“ http://perfecthealthdiet.com/?p=619.
Тук бих добавил, че при сепсис – изключително опасно
възпалително състояние, предизвикано от бактериални инфекции – витамин С коригира
някои от най-тежките симптоми. [5] Ако имате любим човек, който страда
от опасна инфекция, не би било зле да му набавите малко витамин С.
Зависимост на
рециклирането на витамин С от инсулина
DHAA може да се рециклира обратно до витамин С, но само
вътре в клетките.
За да проникне в клетките, DHAA трябва да бъде
транспортирана от глюкозни транспортери. GLUT1, GLUT3 и GLUT4 са трите
транспортера на DHAA при хората; най-активният е GLUT1.
[6]
Транспортът на DHAA е жизненоважен за запасите от витамин
С в мозъка. Няма пряк пренос на витамин С към мозъка, но въпреки това мозъкът е една от
тъканите, които зависят в най-висока степен от този витамин. Той разчита изцяло
на транспорт на DHAA от кръвта с помощта на GLUT1, за да се снабдява с витамин
С. Вътре в мозъка глутатионът трансформира отново DHAA във витамин С.
Ако на пациенти (мишки), получили инсулт, бъде дадена
DHAA дори 3 часа след това, пораженията от инсулта може да се ограничат с до
95%.
DHAA (в доза 250
мг/кг или 500 мг/кг), дадена 3 часа след исхемичния инсулт, намалява засегнатия
от инсулта обем 6 до 9 пъти, като при най-високата доза пораженията се
ограничават едва до 5% от общия обем (Р < 0,05).
[7]
Това е удивително напомняне за значението на витамин С за
зарастването на раните и за превенция на травми.
Глюкозните транспортери се активират от инсулина. Следователно
преносът на DHAA в клетките се повишава от инсулина, което води до по-ефективно
рециклиране на витамин С [8]:
Инсулинът и IGF-1 благоприятстват рециклирането на DHAA
до аскорбин. Source.
В потвърждение на ролята на инсулина за повишаване на
рециклирането на витамин С можем да посочим, че страдащите от диабет тип 1
(които не произвеждат инсулин) имат по-ниски серумни нива на витамин С,
по-високи серумни нива на DHAA, повишена загуба с урината на метаболити на
витамин С и по-голяма нужда от прием на витамин С чрез храната. [9, 10]
Вече можем да предположим какъв е механизмът, по който
нулевият прием на въглехидрати понижава рециклирането на витамин С: като понижават
нивата на инсулина, този вид хранене възпрепятства преноса на DHAA от кръвта към
клетките и така възпрепятства рециклирането на витамин С. Вместо това DHAA се
разгражда, а след това се изхвърля. Вследствие на това организмът губи
витамин С.
Глутатионът и
рециклирането на витамин С
След като влезе в клетката, DHAA се рециклира обратно до
аскорбат, като това се извършва главно от глутатиона в митохондриите:
Глутатионът редуцира
спонтанно, а също така с помощта на ензими, дехидроаскорбата, т.е. напълно
окислената форма на витамин С, в реакции, използващи глутатион или NADPH
(никотинамид-аденин-динуклеотид-фосфат). [11]
Необходим е GLUT1 транспортер върху митохондрената
мембрана, който да транспортира DHAA в митохондриите, като по този начин ефектът
на инсулина върху рециклирането на витамин С може би се повишава значително.
Тъй като глутатионът рециклира витамин С, дефицитът на
глутатион е друга възможна причина за дефицит на витамин С.
Глутатионът се рециклира от ензима глутатион пероксидаза
– съдържащ селен ензим, чието количество зависи от нивата на селен в организма. Един проблем при
диетите с нулев прием на въглехидрати е, че изглежда изчерпват запасите от
селен в организма.
Дефицитът на селен е често срещан страничен ефект на
кетогенното хранене. Има деца с епилепсия, спазвали кетогенно хранене, които са починали от
дефицит на селен! [12]
Така че ето втори механизъм, който допринася за
развитието на скорбут при нулев прием на въглехидрати.
Този хранителен
режим води до дефицит на селен, който провокира дефицит на глутатион, а той
пречи на рециклирането на DHAA обратно до витамин С, което пък води до
разграждане на DHAA и трайна загуба на витамин С.
Заключение
Спазващите хранителен режим с нулев прием на въглехидрати
са застрашени от дефицит на витамин С, дефицит на глутатион и дефицит на селен. Всеки, който има
нулев прием на въглехидрати, трябва да коригира тези дефицити с помощта на
хранителни добавки.
Дефицитите се обострят при хронично ниски нива на
инсулина. Той помага за рециклирането на витамин С, който поддържа запасите от глутатион. Ниският инсулин
повишава разграждането и загубата на витамин С.
Неспособността на организма ефикасно да рециклира витамин
С и да поддържа запаси от антиоксиданти при нулев прием на въглехидрати е
доказателство за това, че еволюционно човекът не е адаптиран към хранене с
нулев прием на въглехидрати.
Не е имало причина предците ни да се адаптират към такъв
начин на хранене. В края на краищата човекът консумира скорбялни храни от
минимум 2 млн. години. Изглежда рисковано да се опитвате да живеете по този начин.
Статии по темата
Други статии от тази серия:
- Dangers of Zero-Carb Diets, I: Can There Be a Carbohydrate Deficiency?.
- Dangers of Zero-Carb Diets, II: Mucus Deficiency and Gastrointestinal Cancers A.
- Dangers of Zero-Carb Diets, IV: Kidney Stones.
Източници
[1]
Willmott NS, Bryan RA. Case report: Scurvy in an epileptic child on a ketogenic
diet with oral complications. Eur Arch Paediatr Dent. 2008
Sep;9(3):148-52. http://pmid.us/18793598.
[2]
Willmott NS, personal communication.
[3]
“Dehydroascorbate,” Wikipedia, http://en.wikipedia.org/wiki/Dehydroascorbate.
[4]
Fain O et al. Hypovitaminosis C in hospitalized patients. Eur J Intern Med.
2003 Nov;14(7):419-425. http://pmid.us/14614974.
[5]
Tyml K et al. Delayed ascorbate bolus protects against maldistribution of
microvascular blood flow in septic rat skeletal muscle. Crit Care Med.
2005 Aug;33(8):1823-8. http://pmid.us/16096461.
[6]
Rivas CI et al. Vitamin C transporters. J Physiol Biochem. 2008
Dec;64(4):357-75. http://pmid.us/19391462.
[7]
Huang J et al. Dehydroascorbic acid, a blood-brain barrier transportable form
of vitamin C, mediates potent cerebroprotection in experimental stroke. Proc
Natl Acad Sci U S A. 2001 Sep 25;98(20):11720-4. http://pmid.us/11573006.
[8]
Qutob S et al. Insulin stimulates vitamin C recycling and ascorbate
accumulation in osteoblastic cells. Endocrinology. 1998 Jan;139(1):51-6.
http://pmid.us/9421397.
[9]
Will JC, Byers T. Does diabetes mellitus increase the
requirement for vitamin C? Nutr Rev. 1996 Jul;54(7):193-202. http://pmid.us/8918139.
[10]
Seghieri G et al. Renal excretion of ascorbic acid in insulin dependent
diabetes mellitus. Int J Vitam Nutr Res. 1994;64(2):119-24. http://pmid.us/7960490.
[11]
Linster CL, Van Schaftingen E. Vitamin C. Biosynthesis, recycling and
degradation in mammals. FEBS J. 2007 Jan;274(1):1-22. http://pmid.us/17222174.
[12]
Bank IM et al. Sudden cardiac death in association with the ketogenic diet. Pediatr
Neurol. 2008 Dec;39(6):429-31. http://pmid.us/19027591. (Hat tip Dr. Deans.)
Рискове при нулев
прием на въглехидрати, част ІV:
Камъни в бъбреците
Автор: Пол Жамине
Бъбречните камъни се срещат често при епилептиците,
спазващи кетогенна диета. [1, 2, 3] Приблизително 1 на 20 деца на
такава диета развива бъбречни камъни всяка година в сравнение с едно на няколко
хиляди сред децата, хранещи се стандартно.
[4] При децата,
които спазват кетогенната диета в продължение на шест години, случаите на
бъбречни камъни са около 25% [5].
100-кратно повишение на заболеваемостта не се наблюдава
почти никога в медицината. Трябва да има някаква фундаментална
причина за възникването на бъбречни камъни, за която клиничните кетогенни диети
допринасят драстично.
Малко повече от половината камъни, образувани при
кетогенно хранене, се състоят от пикочна киселина, а останалите – от калциев
оксалат, примесен с калциев фосфат или пикочна киселина.
Сред неспазващите
кетогенно хранене хора, които развиват бъбречни камъни, около 85% от камъните
са преобладаващо калциево-оксалатни, а около 10% са от пикочна киселина
(уратни). Следователно, грубо казано, уратните бъбречни камъни са
500 пъти по-често срещани при кетогенно хранене, а калциево-оксалатните са 50
пъти по-често срещани.
Причините за възникването
на бъбречни камъни не са добре проучени
В литературата по нефрология бъбречните камъни са доста
загадъчно заболяване.
Уикипедия съдържа списък на посочените в публикации
причини за високата честота на образуване на камъни при кетогенна диета [4]:
Образуването на
бъбречни камъни (нефролитиаза) се асоциира с диетата по четири причини:
·
Излишъкът от калций в урината (хиперкалциурия) възниква поради повишена костна деминерализация в условия на ацидоза. Костите са
изградени основно от калциев фосфат. Той реагира с киселината и калцият се
излъчва от бъбреците.
·
Хипоцитратурия: в урината има необичайно ниска концентрация на цитрат, който обикновено помага
за разтваряне на свободния калций.
·
Урината има ниска киселинност (рН), което пречи на разтварянето на пикочната киселина, а това води до кристали, които действат като нидус - сърцевина, около
която се образуват калциевите камъни.
·
В много болници традиционно са ограничавали приема на вода на пациентите,
спазващи кетогенната диета, до 80% от обичайните дневни нужди. Тази практика
вече не се насърчава.
Това не са удовлетворяващи обяснения. Последните три
фактора наблягат на разтворимостта на пикочната киселина или калция в урината.
Първият – на наличието на калций, един от минералите, които се съдържат в
най-голямо количество в организма.
Не се отчитат източниците на пикочна киселина, оксалат
или калциев фосфат.
Два от факторите наблягат на киселинността на урината, но
ефектът от алкализиращите диети върху образуването на камъни е съвсем скромен. В проучванията
Health Professionals Study и Nurses Health Study I и II, обхващащи към
240 000 здравни работници, участниците, придържали се в най-ниска степен
към диета за понижаване на кръвното налягане от типа DASH (алкализираща диета,
богата на плодове, зеленчуци, ядки и бобови храни), имали риск за развитие на
бъбречни камъни, който бил почти двоен на този при участниците, спазвали
най-стриктно тази диета. [6]
Особено при кетогенни диети приемът на калиев цитрат като
хранителна добавка за алкализиране на урината и осигуряване на цитрат понижава
тройно степента на образуване на камъни. [3] Въпреки това честотата на
нефролитиаза е над 30 пъти по-висока, отколкото при хората, спазващи стандартен
начин на хранене.
Изглежда, че в медицинската общност все още не се
познават някои основни причини за образуването на камъни.
Производство на
пикочна киселина
Една разлика между кетогенната диета (т.е. диетата с
нулев прием на въглехидрати) и стандартният начин на хранене е високата
белтъчна обмяна. Ако и глюкозата, и кетоните се синтезират от протеин, тогава за
глюконеогенезата и кетогенезата се използват над 150 грама протеин на ден. Така се отделя
значително количество азот. Уреята е основният механизъм за
отстраняване на азота, а пикочната киселина е механизмът за елиминиране на 1-3%
азот. [7]
Това навежда на мисълта, че спазващите кетогенно хранене
произвеждат допълнителни 1-3 грама пикочна киселина на ден от белтъчната
обмяна. В обичайния случай един човек излъчва към 0,6 грама на ден.
[8]
Освен бъбречни камъни, производството на пикочната
киселина може да доведе до подагра. Някои от хората, спазващи режима на
Аткинс или нисковъглехидратно палео хранене, са развили подагра.
Производство на
оксалат
В нашата минала
статия (за скорбута) изказахме предположението, че спазващите нисковъглехидратно хранене
вероятно не рециклират витамин С ефикасно от окислената му форма –
дехидроаскорбинова киселина (DHAA).
Ако DHAA не се рециклира до витамин С, то тя се
разгражда. Ето как изглежда процесът на разграждане:
Разграждането на
витамин С при бозайниците започва с хидролизата на дехидроаскорбата до
2,3-дикето- l-гулонат, който се разгражда спонтанно до оксалат,
CO(2) и l-еритрулоза. [9]
Оксалатът е отпадъчен материал, който трябва да бъде
излъчен от бъбреците. Разграждането на витамин С е основен – при инфекциите вероятно най-значимият
– източник на оксалат в бъбреците:
Оксалатът в кръвта
идва от храната, разграждането на аскорбата и синтеза на оксалат в черния дроб и
еритроцитите. [10]
Тъй като скоростта на разграждане на витамин С може да
достигне 100 г/ден при тежки инфекции, а по-голямата част от това количество се излъчва под
формата на оксалат, е очевидно, че ако спазвате стриктна нисковъглехидратна
диета и страдате от активни инфекции, какъвто беше случаят с мен и с К. М. в статията
за скорбута, или сте под друг
вид стрес, който има окислително действие, като например травма или рак, може
спокойно да излъчвате цели грамове оксалат на ден, като това количество се
ограничава от приема на витамин С.
Обезводняване и
загуба на електролити
При излъчването на оксалата се използват и електролити,
основно сол, и вода:
При бозайниците
оксалатът е краен метаболит, който трябва да бъде излъчен или свързан. Бъбреците са
главният орган, който отговаря за излъчването, и са мястото, където оксалатът
изпълнява единствената си функция, която е известна на науката. Той стимулира усвояването
на хлорид, вода и натрий от проксималния тубул чрез обмен на оксалат и
сулфат или хлорид с помощта на транспортера SLC26A6.
[10]
Солта и водата са необходими и на бъбреците за излъчване
на уреята и пикочната киселина.
Аз лично установих, че нуждата ми от сол се повиши
драстично, когато имах нулев прием на въглехидрати.
Нуждаех се от
минимум една чаена лъжичка сол на ден, а когато консумирам въглехидрати, имам
нужда от по-малко от четвърт чаена лъжичка сол.
В резултат на загубата на сол и вода спазващите
нисковъглехидратно хранене често се обезводняват.
Това е често
наблюдаван страничен ефект и на кетогенните диети.
Всички сме виждали какво се случва с урината, когато сме
обезводнени: тя се оцветява заради високите концентрации на разтворени съединения.
С насищането на урината, пикочната киселина и оксалатът
вече не могат да се разтворят. Излъчват се под формата на преципитати
и така създават възможност за образуване на бъбречни камъни.
Полиненаситените
мазнини и бъбречните камъни
Така стигаме до още един фактор, който благоприятства
образуването на бъбречни камъни: високата консумация на полиненаситени
мазнини омега-6.
Ето данните:
Жените в
напреднала възраст (в проучването Nurses Health Study I) с най-висок прием на ЕРА и DHA
имали относителен риск за образуване на бъбречни камъни, равен на 1,28
при мултивариантен анализ (95% доверителен интервал, 1,04 до 1,56; Р за
тенденцията = 0,04), в сравнение с жените с най-нисък прием.
[11]
Консумацията на омега-3 мазнини благоприятства
образуването на калциево-оксалатни камъни кажи-речи толкова, колкото и
консумацията на оксалат. Участниците с най-висок прием под
формата на храна на оксалат имали относителен риск 1,22. [12] (Между другото
най-богатият източник на оксалат е спанакът.)
Но какво в EPA и DHA благоприятства образуването на
бъбречни камъни? Беше ни подсказана една идея от julianne от Julianne’s
Paleo & Zone Nutrition Blog. Тя написа много интересен коментар:
Преди няколко
години започнах да приемам висока доза омега-3 поради възпаление на ставите и
други проблеми. Почувствах голямо облекчение за около 3 месеца, но след това хранителната
добавка спря да ми действа. Разговарях с една приятелка
нутриционистка и тя посочи, че според Андрю Стол (автор на книгата „The Omega 3
Connection“) трябва да приемате 1000 мг витамин С и 500 международни единици
(МЕ) витамин Е дневно, защото в противен случай омега-3 се окислява в организма
ви (в клетъчните мембрани) и губи ефективността си.
Започнах да
приемам и двете добавки и само след няколко дни усетих първоначалното
противовъзпалително действие на омега-3. Оттогава съм разговаряла и с други
хора за това – например, с един психиатър, чиито клиенти се чувствали добре при
прием на омега-3 за 3 месеца, а след това добавката спряла да действа.
В палео общността
често се препоръчва да се приемат високи дози омега-3, а в същото време да се
ограничат въглехидратите. Чудя се дали има хора, които страдат от
дефицит на витамин С вследствие на повишения прием на омега-3 и прекалено
ограничената консумация на въглехидрати?
EPA и DHA имат голям брой нестабилни двойни въглеродни
връзки – съответно по 5 и по 6 – и лесно се окисляват.
Изглежда доста
вероятно това окисляване на мазнините да може да доведе до окисляване и
разграждане на витамин С.
Ако е така, тогава високата консумация на EPA и DHA би
повишила притока на оксалат в бъбреците и би повишила риска за образуване на
калциево-оксалатни камъни. Логично е ефектът да е най-силен при
хората в напреднала възраст, които имат най-ниски нива на антиоксиданти.
Какво ни говори
това за причината за камъните при хранещите се стандартно хора?
Тъй като повечето бъбречни камъни, които се откриват при
хранещите се стандартно хора, са калциево-оксалатни, изглежда вероятно
разграждането на витамин С да е основният източник на суровини за образуване на
бъбречни камъни.
Ако това е вярно, то тогава рискът за образуване на
камъни може да се понижи чувствително с подходящ хранителен режим и прием на
хранителни добавки.
Първо, степента на окисление може да се понижи чрез
по-висок прием на антиоксиданти като:
- глутатион и неговите прекурсори като Н-ацетилцистеин;
- селен заради глутатион пероксидазата;
- цинк и мед заради супероксид дисмутазата;
- коензим Q10 за защита на липидите;
- алфа-липоева киселина;
- разноцветни зеленчуци и горски плодове.
Приемът на витамин С има и положителни, и отрицателни
ефекти: антиоксидантното му действие е благоприятно, но разграждането му е вредно.
Второ, приемът на електролити и вода е важен. Особено важна е солта.
На последно място, алкализиращите компоненти като лимонов
сок или други източници на цитрат, могат да повишат разтворимостта на пикочната
киселина.
Заключение
Спазващите диета с нулев прием на въглехидрати имат
повишен риск за:
- прекомерно ниво на оксалат от бъбреците заради неспособност за рециклиране на витамин С;
- прекомерно ниво на пикочна киселина от бъбреците заради елиминиране на азотни продукти от глюконеогенезата и кетогенезата;
- дефицит на сол и други електролити заради излъчване на оксалат, урея и пикочна киселина; и
- обезводняване.
Тези четири състояния драстично повишават риска за
образуване на бъбречни камъни.
За да ги коригирате, препоръчваме на всички, които
спазват периодично гладуване или диета с нулев прием на въглехидрати, да приемат
антиоксиданти под формата на храна или хранителни добавки, да консумират сол и
други електролити и да пият много вода.
Също така, освен ако не съществува терапевтична причина
за ограничаване на въглехидратите, е най-добре 20% от калориите ви за деня да
идват от въглехидрати, за да понижите нуждата от синтез на глюкоза и кетони от
протеин. Така значително ще понижите излъчването на пикочна киселина. Освен това ще
понижите и разграждането на витамин С, както твърдим в миналата си статия, а така значително ще ограничите и излъчването на оксалат.
Статии по темата
Други статии от тази серия:
- Dangers of Zero-Carb Diets, I: Can There Be a Carbohydrate Deficiency?.
- Dangers of Zero-Carb Diets, II: Mucus Deficiency and Gastrointestinal Cancers A.
- Danger of Zero-Carb Diets III: Scurvy .
Източници
[1]
Furth SL et al. Risk factors for urolithiasis in children on the ketogenic
diet. Pediatr Nephrol. 2000 Nov;15(1-2):125-8. http://pmid.us/11095028.
[2]
Herzberg GZ et al. Urolithiasis associated with the ketogenic diet. J
Pediatr. 1990 Nov;117(5):743-5. http://pmid.us/2231206.
[3]
Sampath A et al. Kidney stones and the ketogenic diet: risk factors and
prevention. J Child Neurol. 2007 Apr;22(4):375-8. http://pmid.us/17621514.
[4]
“Ketogenic diet,” Wikipedia, http://en.wikipedia.org/wiki/Ketogenic_diet.
[5]
Groesbeck DK et al. Long-term use of the ketogenic diet. Dev Med Child
Neurol. 2006 Dec;48(12):978-81. http://pmid.us/17109786.
[6]
Taylor EN et al. DASH-style diet associates with reduced risk for kidney
stones. J Am Soc Nephrol. 2009 Oct;20(10):2253-9. http://pmid.us/19679672.
[7]
Gutman AB. Significance of uric acid as a nitrogenous waste in vertebrate
evolution. Arthritis Rheum. 1965 Oct;8(5):614-26. http://pmid.us/5892984.
[8]
Boyle JA et al. Serum uric acid levels in normal pregnancy with observations on
the renal excretion of urate in pregnancy. J Clin Pathol. 1966
Sep;19(5):501-3. http://pmid.us/5919366.
[9]
Linster CL, Van Schaftingen E. Vitamin C. Biosynthesis, recycling and
degradation in mammals. FEBS J. 2007 Jan;274(1):1-22. http://pmid.us/17222174.
[10]
Marengo SR, Romani AM. Oxalate in renal stone disease: the terminal metabolite
that just won’t go away. Nat Clin Pract Nephrol. 2008 Jul;4(7):368-77. http://pmid.us/18523430.
[11]
Taylor EN et al. Fatty acid intake and incident nephrolithiasis. Am J Kidney
Dis. 2005 Feb;45(2):267-74. http://pmid.us/15685503.
[12]
Taylor EN, Curhan GC. Oxalate intake and the risk for nephrolithiasis. J Am
Soc Nephrol. 2007 Jul;18(7):2198-204. http://pmid.us/17538185.